Dr. Stefaan Van Gool, MD, PhD, ist als international anerkannter Experte für Tumorimmunologie sowie Neuroonkologie bei Kindern und Erwachsenen als medizinischer Direktor der Praxis für Immunonkologie & Translationale Medizin im Deutschen Immunonkologischen Zentrum in Köln tätig. Mit Unterstützung des Nobelpreisträgers Professor Steinman initiierte Dr. Stefaan Van Gool die wegweisende Forschung zu dendritischen Zellen in der Tumortherapie und war damit einer der ersten Ärzte in Europa, der einen Patienten mit Glioblastom mittels dendritischer Zell-Immuntherapie behandelte. Seine berufliche Laufbahn konzentriert sich konsequent auf ein zentrales Prinzip: die individualisierte multimodale Immuntherapie.
Individualisierte multimodale Immuntherapie in einem therapeutischen Gesamtkonzept
Nach der Diagnose eines soliden Tumors oder eines Hirntumors besteht der erste Behandlungsschritt in der Standardtherapie. Diese umfasst chirurgische Eingriffe, Strahlentherapie und/oder Chemotherapie mit dem Ziel, die Tumormasse so weit wie möglich zu reduzieren. Bleiben jedoch Tumorzellen unbehandelt zurück, besteht ein hohes Risiko für ein Wiederauftreten der Krebserkrankung. Neu entwickelte Therapieansätze setzen daher gezielt auf die Aktivierung des körpereigenen Immunsystems. Die Anwendung des eigenen Immunsystems wird als „individualisierte Immuntherapie“ bezeichnet. Da die Immuntherapie aus verschiedenen Techniken besteht, wird deren Kombination als „multimodale Immuntherapie“ bezeichnet. Die gezielte Kombination mehrerer immunstimulierender Verfahren wird als individualisierte multimodale Immuntherapie (IMI) bezeichnet.
Die Immuntherapie wird durch drei wesentliche Faktoren erschwert:
1. Erstens ist das Immunsystem darauf trainiert, körpereigene Zellen nicht anzugreifen. Genau aus solchen Zellen besteht ein Tumor.
2. Zweitens kann sich der Tumor dem Immunsystem entziehen oder dieses aktiv unterdrücken.
3. Drittens schwächen Strahlen- und Chemotherapie neben dem Tumor auch das Immunsystem.
Aus diesem Grund ist es entscheidend, verschiedene Therapieformen in mehreren aufeinanderfolgenden Phasen einzusetzen: Zunächst wird der Tumor selbst geschwächt, anschließend das Immunsystem wieder aufgebaut und schließlich gezielt trainiert und gegen den fortschreitenden Tumor aktiviert. Für jeden Patienten muss daher ein übergeordnetes therapeutisches Gesamtkonzept erstellt werden.
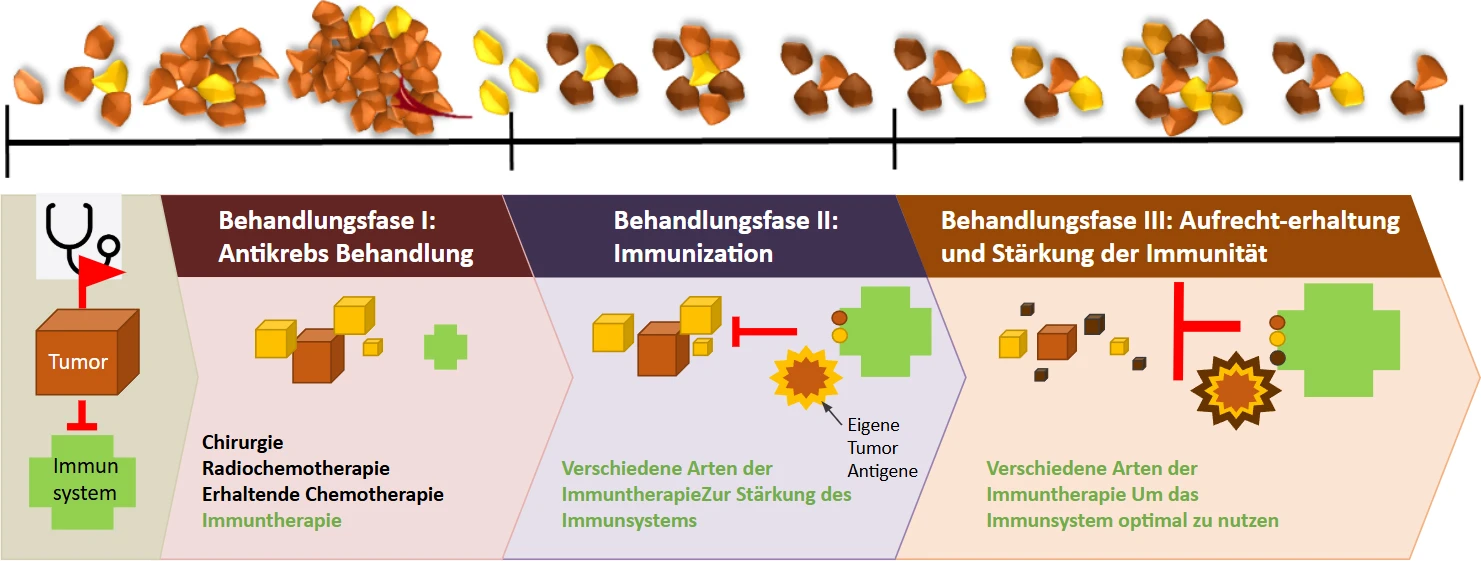
Die verschiedenen Therapiephasen
In der ersten Phase der Krebstherapie wird der Tumor mittels Standardbehandlung angegangen. Radio- und Chemotherapie schwächen den Tumor, aber auch das Immunsystem. Bereits in dieser Phase können immuntherapeutische Verfahren ergänzt werden, um Tumorzellen gezielt zu zerstören und das Tumormikromilieu zu verändern. Die Patienten erhalten eine modulierte Elektrohyperthermie, bei der elektromagnetische Wellen gezielt durch den Tumor geleitet werden. Da Tumorzellen metabolisch aktiver sind als gesunde Zellen, reagieren sie empfindlicher auf Hitzestress und werden selektiv zerstört. Zusätzlich werden Injektionen des sogenannten Newcastle-Disease-Virus verabreicht. Das Virus, das normalerweise ausschließlich Vögel infiziert, kann jedoch auch Tumorzellen befallen, da diese ihre antiviralen Schutzmechanismen verloren haben. Das Virus zerstört den Tumor von innen heraus und schafft zugleich neue Angriffspunkte für das Immunsystem.
In der zweiten Phase wird aktiv eine antitumorale Immunantwort durch Impfungen aufgebaut. Hierzu werden dendritische Zellen eingesetzt, Schlüsselzellen des Immunsystems, welche andere Immunzellen aktivieren und so eine gezielte Immunreaktion auslösen. Diese patienteneigenen dendritischen Zellen werden im Labor gewonnen und mit patienteneigenen Tumorzellen sowie Tumorbestandteilen, sogenannten Antigenen, beladen, sodass sie den Tumor als Bedrohung erkennen lernen. Nach der Reinfusion in den Körper aktivieren sie das Immunsystem. Da sich Tumorzellen der Immunerkennung entziehen können, kommen zusätzlich Checkpoint-Inhibitoren zum Einsatz. Diese blockieren hemmende Signalwege auf Tumor- oder Immunzellen, sodass die Immunzellen ihre Funktion effektiv ausüben können.
Da sich Tumoren kontinuierlich weiterentwickeln, um immunologischen Angriffen zu entgehen, wird in der dritten Phase das Immunsystem dauerhaft aktiviert und weiter gestärkt. Ziel ist es, den Tumor wiederholt und auf unterschiedliche Weise anzugreifen.
Die Wirkung
Die individualisierte multimodale Immuntherapie wird für jeden Patienten maßgeschneidert konzipiert. Dabei werden die spezifischen Eigenschaften des Tumors, vorhandene Mutationen, bereits durchgeführte Behandlungen sowie der Immunstatus des Patienten berücksichtigt. Für jeden Patienten wird individuell festgelegt, welche therapeutischen Maßnahmen zu welchem Zeitpunkt den größten Nutzen versprechen. Dies führt dazu, dass keine zusätzliche Toxizität entsteht: Es werden ausschließlich körpereigene Immunzellen und patienteneigene Tumorzellen verwendet, um das Immunsystem zu trainieren und zu stärken.
Dr. Stefaan Van Gool: „Betrachtet man Patientengruppen, zeigt sich insbesondere bei Hirntumorpatienten, speziell bei Glioblastom-Patienten, eine deutliche Verlängerung der durchschnittlichen Lebenserwartung bei Einsatz von IMI. Während unter alleiniger Standardtherapie eine durchschnittliche Überlebenszeit von weniger als zwei Jahren zu erwarten ist, zeigt sich bei zusätzlicher IMI nahezu eine Verdopplung der durchschnittlichen Überlebensdauer. Dieser Effekt ist weder bei Einzeltherapien noch bei gleichzeitig kombinierten Therapien zu beobachten und unterstreicht die Bedeutung einer zeitlich abgestuften therapeutischen Strategie.
Neben der Lebenserwartung ist auch die Lebensqualität ein zentraler Bewertungsmaßstab für den Wert einer Therapie. Daher werden Patienten regelmäßig gebeten, standardisierte Fragebögen zur Selbsteinschätzung auszufüllen. Diese Daten zeigen, dass die Lebensqualität bei vielen Patienten während der IMI stabil bleibt und sich bei einem Teil der Patienten sogar verbessert, unabhängig von der Therapiedauer oder dem individuellen Behandlungsplan. Selbst bei einem Tumorrezidiv, das häufig mit einer deutlichen Verschlechterung der Lebensqualität einhergeht, trägt die IMI dazu bei, diese aufrechtzuerhalten.
Damit können wir wissenschaftlich feststellen, dass jeder Tag, der mit Hilfe von IMI gewonnen wurde, auch wirklich gelebt werden kann.“
IMI als Teil der Standardbehandlung?
Derzeit sind viele immuntherapeutische Verfahren, einschließlich der IMI, ausschließlich im Rahmen privater Behandlungen oder klinischer Studien verfügbar und noch nicht Bestandteil der Regelversorgung. Behandlungen, die unter die Standardversorgung fallen, sind für Patienten zugänglich, da sie direkt von Onkologen empfohlen werden und die Kosten von den Krankenkassen übernommen werden. Dadurch wird die Immuntherapie häufig erst spät eingesetzt oder bleibt aus finanziellen Gründen oder aufgrund mangelnder Bekanntheit für viele Patienten unzugänglich. Eine Integration der IMI in die Regelversorgung könnte diese Probleme lösen. Doch welche Hürden bestehen?
Therapien werden nur dann in die Regelversorgung aufgenommen, wenn sie auf Grundlage ausreichender Evidenz als sicher und wirksam gelten. Der Nachweis erfolgt über ein komplexes und kostenintensives System: randomisierter klinischer Studien. Diese Studien gliedern sich in mehrere Phasen: In Phase I wird die Sicherheit einer Therapie geprüft, in Phase II deren Wirksamkeit. Diese Phasen werden häufig kombiniert und an einer kleinen, gut informierten Patientengruppe durchgeführt. In Phase III wird die Therapie an einer sehr großen Gruppe getestet, bestehend aus Patienten und gesunden Probanden, die blind entweder ein Placebo oder die Therapie erhalten. Diese Phase erstreckt sich oft über mehrere Jahre und ist mit erheblichen Kosten verbunden.
Dieses System bietet zwar Vorteile, bringt jedoch auch erhebliche Nachteile mit sich. Die strengen Einschlusskriterien in Bezug auf z.B. Alter, Gesundheitszustand, andere Behandlungsformen und Tumoreigenschaften, schließen viele Patienten aus. Auch der zeitliche Aufwand führt dazu, dass zahlreiche Betroffene keinen Zugang erhalten. In einigen Ländern dürfen Patienten erst dann an Studien teilnehmen, wenn alle Standardtherapien ausgeschöpft sind; ein gravierendes Problem, wenn diese länger dauern als die durchschnittliche Lebenserwartung. Personalisierte und individualisierte Therapien, deren Bedeutung mit zunehmendem Wissen über tumorindividuelle Unterschiede wächst, lassen sich kaum innerhalb standardisierter Studienprotokolle evaluieren. Vielleicht sollten wir uns auch fragen: Sind feste klinische Studienprotokolle der richtige Weg, um hochdynamische, unkontrollierte Tumoren zu bekämpfen? Zudem sind standardisierte Therapien wirtschaftlich attraktiver, da sie skalierbar sind. Individualisierte Therapien hingegen müssen für jeden Patienten separat entwickelt werden, was die Kosten erheblich erhöht, vor allem, wenn sich eine teure Entwicklungsphase amortisieren muss. Trotz nachgewiesener Sicherheit und Wirksamkeit erreichen daher nur 3,4 % der in klinischen Studien getesteten Krebstherapien letztlich den Patienten.
Trotz dieser Einschränkungen gelten klinische Studien weiterhin als Voraussetzung für die Aufnahme in die Regelversorgung. Da sich die Wissenschaft schneller entwickelt als die regulatorischen Prozesse, ist eine erhebliche Lücke zwischen dem medizinisch Machbaren und dem regulatorisch Erlaubten entstanden. In der Behandlung von Glioblastom-Patienten ist die Standardtherapie seit über 20 Jahren unverändert, obwohl sie nicht bei allen Patienten wirksam ist und trotz erheblicher wissenschaftlicher Fortschritte. In Ländern wie Deutschland besteht jedoch die Möglichkeit, Therapien außerhalb der Regelversorgung im Rahmen des „Individueller Heilversuchs“ in Anspruch zu nehmen. Der Patient wird umfassend aufgeklärt und entscheidet selbst über die Behandlung. Dadurch sind in Deutschland fortschrittlichere Krebstherapien doch zugänglich.
Im Rahmen des individueller Heilversuchs gelten weniger Restriktionen als bei klinischen Studien. Die dabei erhobenen Daten, sogenannte Real-World-Daten, spiegeln häufig die klinische Realität besser wider als hochselektierte Studienpopulationen. Sollten diese Daten künftig als Evidenz für die Aufnahme neuer Therapien in die Regelversorgung anerkannt werden, eröffnen sich neue Perspektiven für Krebspatienten. Der Weg dorthin ist jedoch noch lang.
Das Bestreben von Dr. Stefaan Van Gool
Dr. Stefaan Van Gool ist bei seinen Patienten und Mitarbeitern als äußerst kompetenter und zugleich sehr einfühlsamer Arzt bekannt. Patienten aus aller Welt suchen ihn aufgrund seiner herausragenden Expertise in der individualisierten Krebsbehandlung auf. Neben der direkten Patientenversorgung setzt sich Dr. Van Gool intensiv dafür ein, den Nachweis der Wirksamkeit der IMI auf Basis von Real-World-Daten aus seiner eigenen Praxis für Patienten mit soliden Tumoren und Hirntumoren international zugänglich zu machen. Gemeinsam mit seinem Team arbeitet er zudem an der regulatorischen Anerkennung von Real-World-Evidenz, um innovative Therapieansätze weltweit schneller für alle Patienten verfügbar zu machen.

